Este artículo es parte de la edición de enero, 2022
Nuevas vacunas frente a la influenza aviar
ELÍAS F. RODRÍGUEZ FERRI Dr. Veterinario. Facultad de Veterinaria de León
La influenza aviar (peste aviar o gripe aviar, por otras denominaciones) es, sin duda alguna, la más importante enfermedad infecciosa de las aves y la que mayor preocupación genera entre avicultores y técnicos veterinarios, en general.
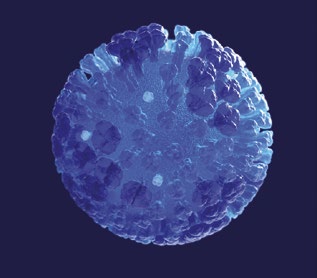
Producida por un Orthomyxovirus Influenza A, su agente causal puede presentarse como un virus de baja patogenicidad (LPAI –Low Pathogenicity Avian Influenza-) o de alta patogenicidad (HPAI –High Pathogenicity Avian Influenza-), capaz de producir la muerte de gallinas o pavos, por ejemplo, en un 100% de los efectivos, en 24 horas, sin apenas síntomas previos o, por el contrario, comportarse como un virus respiratorio sin consecuencias graves, con la particularidad de que en algunas ocasiones comienza como LPAI y evoluciona a HPAI, como ya ha ocurrido en el pasado.
El responsable de estas variaciones en la patogenicidad es una gran plasticidad evolutiva basada en su capacidad para mutar, que produce pequeños cambios acumulativos en el genoma.

Alternativamente, también a cambios más sustanciales debido a un proceso de reordenación o reagrupamiento genómico como consecuencia de la mezcla de los segmentos que forman su genoma de ARNmc de sentido negativo, que codifican para 8 proteínas estructurales, cuando se produce coinfección celular. El sistema de clasificación tradicional de estos virus utiliza la combinación de las dos proteínas principales (hemaglutinina y neuraminidasa) para formar un elevado número de subtipos HN (hasta 144 posibles, sin considerar los tipos de HA y NA correspondientes a los murciélagos) y dentro de ellos todavía se establecen linajes, variantes, clados o subclados debido a cambios en éstas y en alguna de las otras proteínas (3 polimerasas, -PA, PB1 y PB-2-, 2 proteínas de la matriz –PM1 y PM2- y la NP, a lo que se suman otras proteínas no estructurales) que en la práctica representan una capacidad de variación extraordinaria con consecuencias en muchos aspectos, incluida la patogenicidad. Alguno de los 8 segmentos genómicos, mediante un sistema de marco de lectura alternativo y splicing del ARNm codifican para más de una proteína alcanzando así la capacidad de expresión de un total hasta de 13 proteínas.

Tradicionalmente, la presencia de la HA 5 y HA7, en distintas combinaciones, se asocia a la patogenicidad elevada. En la actualidad, varios países europeos, sufren brotes repetidos por la intervención de un subtipo H9N2, LPAI que, además de ser endémico aquí, lo es también en Asia y en África. Pese a la condición de LPAI, es capaz de infectar al hombre y otros mamíferos, como sucede con el cerdo1. El virus se aisló de pavos, por primera vez, en los EE.UU. en 1966 y en 1998 se describió su capacidad para infectar al hombre en varios brotes que sucedieron en China2,3. En las aves origina problemas en la producción de huevos, en forma de reducción de la calidad y producción, así como en un incremento de la mortalidad común, esperada. En gallinas con infecciones no complicadas origina pérdida de peso con formas anormales en el huevo, cáscaras débiles y hemorragias masivas en ovarios, oviducto y otros órganos importantes. La disminución de la producción de huevos puede ser debida al proceso de replicación en el tracto reproductor (infundibulum) que origina lesiones desde agudas a crónicas. Además, se ha comprobado que el H9N2 es donador común de genes en varios subtipos, incluyendo el HPAI H5N1 o el H7NX y, cuando existe cocirculación de cualquiera de ambos tipos, naturalmente HPAI, se producen cambios o modificaciones por reordenamiento que pueden afectar a la patogenicidad, incrementándola, así como a la transmisión más eficiente a mamíferos5, con lo que el riesgo aumenta tanto en el sentido de la sanidad animal como de la salud pública.
ADEMÁS, EN REGIONES DONDE SE PRODUCEN BROTES DE ENFERMEDADES SIMULTÁNEAS POR OTRAS ETIOLOGÍAS, COMO NEWCASTLE, BRONQUITIS O INFECCIONES BACTERIANAS, PUEDEN PRODUCIRSE PROCESOS DE RECOMBINACIÓN HETERÓLOGA E INTERCAMBIOS GENÓMICOS ENTRE SUBTIPOS DE INFLUENZA, POR EJEMPLO, H5N1, CON CONSECUENCIAS GRAVES.
La mayor parte de las vacunas disponibles en la actualidad frente a la influenza aviar son inactivadas de diversos formatos, muy seguras, pero que adolecen del inconveniente de la pérdida o modificación de antígenos importantes durante el proceso de inactivación. Son, por el momento, muy escasos los ejemplos de plataformas para la producción de vacunas recombinante o vectoriales que tan comunes están siendo en el uso de algunas otras enfermedades de animales, mamíferos o aves, para producir antígenos purificados (ordinariamente de la HA en el caso de la influenza aviar) en formulaciones simples o mixtas, como sucede en el caso de una vacuna recombinante que combina la HA del subtipo H5N1 con La Sota, de la enfermedad de Newcastle. En condiciones experimentales, también, se ha descrito un replicón del virus de la encefalitis equina que incorpora una hemaglutinina, también con resultados alentadores, más que en algunos ensayos realizados en una propuesta de vacuna de ADN.

Otra condición deseable, sobre todo en los programas de vigilancia, es el uso de vacunas que sean capaces de diferenciar el resultado de la vacunación de los estados de infección en lo que a las respuestas inmunitarias humorales se refiere, las conocidas vacunas DIVA (Differentiate Infected from Vaccinated Animals) que diferencian en las respuestas serológicas los anticuerpos debidos a la vacunación de aquellos procedentes de los estados de infección. En los casos de las vacunas de influenza una de las opciones más comunes es cambiar la neuraminidasa de la fórmula vacunal por otra diferente que actúa como marcador o centinela, aunque también se han utilizado o propuesto otras alternativas como la proteína no estructural 1 (NS1), un ectodominio de la proteína de la matriz 2 (M2e) o la subunidad 2 de la hemaglutinina (HA2).
Recientemente investigadores del Instituto Pirbright, del Reino Unido, han desarrollado una nueva vacuna experimental basada en un sistema direccional para la hemaglutinina recombinante del H9N2 dirigidas a células dendríticas de pollo, presentadoras de antígeno, mediante su conjugación con un fragmento funcional de la porción variable de las cadenas pesadas y ligeras de inmunoglobulinas anticuerpo scFv dirigidas frente al receptor celular CD836.
Los resultados del estudio fueron en extremo interesantes pues el scFv r HA9-CD83 indujo anticuerpos en niveles elevados en tiempos tan precoces como 6 días después de la vacunación, siendo capaces, además, de reducir sustancialmente la eliminación de virus cuando se compararon con el recombinante de HA no conjugado, y el fragmento de anticuerpo (scFV CD83), igual que sucedió en el caso de una vacuna inactivada de virus completo H9N2. Los recombinantes se expresaron en una plataforma de células S2 de Drosophila malanogaster con purificación posterior por cromatografía de afinidad.
ESTA TECNOLOGÍA, QUE YA SE CONOCE BIEN EN OTRAS APLICACIONES MÉDICAS, PUEDE CONTRIBUIR A MEJORAR LA EFICACIA DE ESTOS PRODUCTOS E INCLUSO A ESTABLECER PROCEDIMIENTOS QUE COMBINEN CON VENTAJA VARIOS ANTÍGENOS PROMOVIENDO MEJORES RESULTADOS EN LA RESPUESTA VACUNAL.
1WHO Regional Office for Europe Overview on avian influenza for Public Health Professionals. WHO. Geneva, Switzerland, 2015
2Peiris M, Yuen KY, Leung CW, et al. Infection with Influenza H9N2. Lancet 1999; 354: 916-917
3Ma C, Cui S, Sun Y, Zhao J, et al. Avian influenza A (H9N2) virus infections among poultry workers, swine workers and the general population in Beijing. China, 2013-2016. A serological cohort study. Influenza Other Resp Viruses 2019; 13: 415-425
4Jonas M, Sahesti A, Murwijati T, Lestariningsih CI, et al., Identification of avian influenza virus subtype H9N2 in chicken farms in Indonesia. Prev Vet Med 2018; 159: 99-105
5Arai Y, Ibrahim MS, Elgendy EM, Daidoji T, et al., Genetic compatibility of reassortants between avian H5N1 and H9N2 Influenza viruses with Higher Pathogenicity in mammals. J Virol 2018; 93 (4): e01969-18.
6Shrestha A, Sadeyen JR, Lukosaityte D, Chang P, et al. Selective targeting haemagglutinin antigen to chicken CD83 receptor induce faster and stronger immunity against avian influenza. npj Vaccines 2021; 6:90 doi 10.1038/s41541-021-00350-3
Con el apoyo de:

Categorías

Clasificados enero 2022
Leer
La carne de ave española se promociona en los EAU
Leer
La feria de El Prat de Llobregat, celebrada con PCR para descartar la influenza aviar
Leer
Grupo AN colabora con Eroski para lanzar etiquetas inteligentes en productos avícolas
Leer
Una planta de incubación y una docena de granjas se volatilizan por tornados en EE.UU.
Leer
El riesgo de transmisión aérea de la influenza aviar de las aves acuáticas silvestres a las aves domésticas es insignificante
Leer
 Revistas
Revistas Archivo
Archivo La revista de la industria
La revista de la industria










































 PDF
PDF